科室介绍 查看全部
科室医生 查看全部
科普·直播义诊专区 查看全部
- 精选 立体定向放射治疗(SRS)
1、常规放射治疗的特点:常规放射治疗是各大医院放射治疗科的主要工作,包括x线机定位的二维常规放疗、CT定位的三维适形放疗以及现在主流的调强适形放疗等。一是把肿瘤做为一个体积来治疗,同时对相应的淋巴结引流区做预防照射;二是照射野设计在同一个平面(共面照射),具有剂量均匀不容易出现低剂量区的特点(剂量不足往往是肿瘤复发的主要原因);三是采用常规分割剂量(每天一次,每次2GY,每周5次);2、立体定向放射治疗(SRT)的特点:是指那些通常称为“刀”的放射治疗,目前所用名称比较多,但大体都属于SRT的范畴,包括高剂量分割照射(hyperfractionradiotherapy,HFRT、体部立体定向放射治疗SBRT(StereotacticBodyRadiationTherapy)、立体定向放射外科(SRS,包括x刀和伽马刀),应该说,只有做一两次性损毁性照射的SRT才能称之为“刀”(SRS),所以,SRS也可以看作是SRT的一个特殊情况。SRT具有一下特点:一是可以把它看作是常规放射治疗的一个特例,也就是把照射部位做为一个点来照射而不是一个体积,所以照射区域一般都在3㎝一下;二是照射野设计可以是单一共面也可以是多共面(非共面),将射线从不同方向、不同角度聚焦到照射区域,具有中心剂量很高而周围正常组织剂量低的特点;三是单次剂量大(3~15GY,但没有固定的剂量规定)、照射次数少(1~15次不等,也没有具体多少次的规定);总的特点是中心剂量大、周边剂量小、剂量落差大、剂量分布不均匀。3、哪些疾病适合做哪种方式的放射治疗?3.1常规放疗治疗仍是恶性肿瘤治疗的主要模式,绝大部分恶性肿瘤都适合做常规放疗而不是“刀”,尤其是需要做区域淋巴结预防的患者;3.2.1部分常规放疗不敏感的肿瘤和常规放疗失败的肿瘤适合做SRS,比如颅内的多数良性又不便于手术切除的肿瘤、不适合手术的周围型肺癌、常规放疗失败的胶质瘤、脑部的脑转移瘤等;3.2.2还有像脑血管畸形只需要经过放疗,损伤血管内皮细胞,导致畸形的血管萎缩不再出血就可以了、垂体瘤只需要不再分泌过量的激素就可以了,听神经瘤和脑膜瘤等良性肿瘤只要控制其生长不对周围组织造成压迫就可以了,也适合做SRT治疗;3.2.3还有有确切病灶的癫痫患者以及一些特殊的脑功能疾病,也适合做SRS治疗。4、立体定向放射治疗的趋势是什么?4.1很长时间以来,做经典放疗的医生和做“刀”的医生缺乏共识,但现在,大家对SRT都有了比较好的认同感,一是因为有些常规放疗不敏感的肿瘤通过SRT可以获得好的生物学效应和好的治疗结果,二是多分次的大分割治疗同样可以达到一次性损毁治疗的目的(功能和组织损毁程度决定于组织的α/β比值和总生物学剂量,而不是次数多少),同时又能避免SRT一次性治疗的诸多风险。以前做一次性治疗的目的除了单次大剂量有更高的生物学效应外,病人长时间带头架也是很痛苦和不现实的,每次放疗过程也非常麻烦,需要尽早完成治疗。4.2伽马刀所用的射线是钴60同位素释放的伽马线,无论关机与否它都在释放射线,不容易防护,容易出现照射事故,而x刀用的是直线加速器的x线,一关机就没有射线了,很容易防护;同位素释放出的伽马线有不断衰变的特点,每次治疗是需要根据放射源的出产日期和半衰期进行能量计算,而直销加速器就没有这些麻烦;另外,近几年随着计算机和数字化程度的提高,加速器的治疗精度得到了很大提高,误差可以达到0.5㎜级,再加上先进的直线加速器还自带CT,每次治疗前都可以做一次位置确定和校准,目前的发展方向是x刀的应用越来越多。5、立体定向放射治疗有哪些副作用和风险?治疗期间的急性副作用是恶心呕吐和头部不适,会很快缓解,之后也是最重要的副作用是放射性水肿,多出现在3~36个月之间,有症状者需要脱水、利尿和激素治疗,其它还有瘤体出血、放射性坏死空洞形成和继发性癫痫等可能。
张俊德 主任医师 南方医科大学珠江医院 放疗科1.5万人已读 - 精选 全中枢放疗(全脑全脊髓放疗)
适应症:有脑脊液播散的中枢神经肿瘤,包括以髓母细胞瘤为代表的原发中枢神经系统胚胎性肿瘤、部分室管膜瘤、部分生殖细胞瘤和中枢神经系统淋巴瘤,以及各种沿脑脊液播散的肿瘤。照射范围和剂量:包括全脑+全脊髓,剂量范围根据病种和分级的不同在23.4GY~36GY左右(13~20次,全脑全脊髓照射完成后再对脑部的可见病灶或者手术区域补量,局部追加的剂量也因为病种的不同而不同,例如髓母细胞瘤需要追加至总剂量54GY(共计29次,生殖细胞瘤约需40~54GY(22~27次,淋巴瘤约50GY。全脑全脊髓放疗一是要照全所有有脑脊液的地方,直回、球后、筛板、颅神经出颅的地方以及肋间神经和骶神经出髓腔的地方特别容易遗漏;二是能不照射的地方尽量避免照射或少照射,以减少对血象、生长发育以及生育能力的影响。需要注意的问题:1.放疗期间的反应。开始几次时患者可能会有头部闷胀不适、头晕等,乏力和疲劳感,胃口差,腹部隐隐不适等,全中枢放疗后期有咽部不适、咽喉痛和刺激性咳嗽等。但放疗期间医生更关心的是血象问题。2.脊髓损伤的预防。低位的脊髓损伤会导致瘫痪和大小便困难,高位的损伤甚至会导致死亡。脊髓是串联器官,正常脊髓对放射线的耐受剂量有限,总的来说年龄越小耐受性越差、越是上段耐受性越差、照射长度越长耐受性越差,一般是一个椎体长度的脊髓是50GY,10公分长度为45GY,全脊髓放疗一般都控制在36GY以内。另外,加速器的射野最大为4040cm大小,全中枢照射是需要2~3个照射野衔接的。因为射线有5度左右的发射,尽量避免用普通放疗,而是用三维适型或调強适形放疗来做剂量衔接,避免衔接部位照射遗漏导致的疾病控制不佳,或者照射野重叠导致的脊髓损伤,就算是这样,每周还得更换一次衔接位置。做过全中枢放疗的患者要慎用MTX鞘内注射,会增加脱髓鞘的风险。3.血象问题.椎骨是重要的造血组织,全中枢大范围的造血骨受到照射,一定会出现白细胞和血小板的降低,甚至有血小板重度减少导致死亡的报道,全中枢放疗也会导致放疗后再做化疗时的耐受性降低,所以在整个放疗期间需要每周检测血象,并谨慎加用化疗药物(在血象允许的情况下,髓母细胞瘤患者要求每周静脉用一次长春新碱,1.4mg/m2)。4.生长发育问题:需要全中枢照射的患者多为儿童,生长发育问题、智力问题和生育问题都必须引起足够的重视。理论上来说,椎体骨受到10GY以上剂量的照射都可能出现骨发育停止,长大成人后可能会出现上身略短、下身略长的比例失调;另外,做放疗计划时需要照射整个椎体,防止在今后的生长过程中椎体畸形。5.智力问题。智力问题主要是全脑放疗带来的影响。理论上来讲做过全脑放疗后的智力多多少少会受到影响,包括学习理解能力下降、情感甚至认知力下降等,但人常生活没有影响,我们10年前全脑放疗的小孩这几年都陆续考上大学甚至是重点大学。尽管如此,对年龄很小大脑发育还没有完成的儿童、对老年人尤其是已经有认知功能障碍的老年人做全脑放疗仍需权衡利弊。6.生育问题。包括两个方面的影响,一是内分泌功能的影响,更重要的是不能让女孩的卵巢受到照射(男孩的睾丸是受不到照射的),所以在设计照射野时最下面一个照射野需要用侧野而不是前后野照射。
张俊德 主任医师 南方医科大学珠江医院 放疗科1.6万人已读 - 精选 胶质瘤治疗有哪些办法和困难?
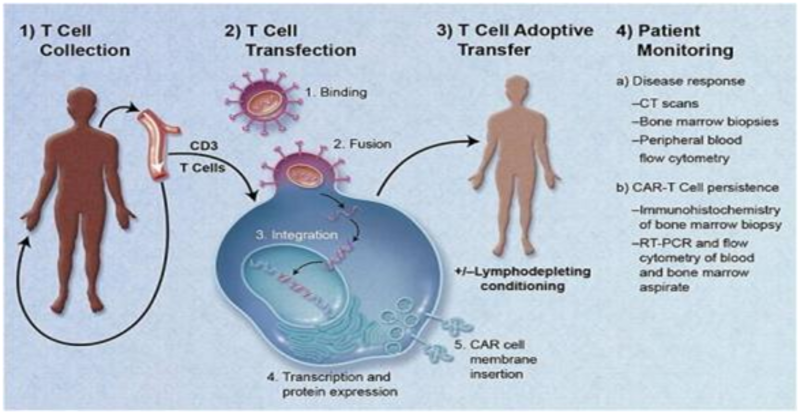
胶质瘤是主要生长在大脑半球、发生于神经间质细胞的恶性肿瘤,进展快、预后不良,虽然近年来取得了很多进展,但疗效仍远不如人意;例如,四级的胶质母细胞瘤平均生存期只有14个月(手术的贡献2-3个月,放疗2-3个月,化疗2-3个月,贝伐单抗3-4个月,对症支持治疗和其它约2-3个月)。现将胶质瘤治疗的主要方法和困难总结如下,希望能帮助到患者。 1.手术:手术治疗仍然是胶质瘤的首要治疗,一是病人就诊时都有了明显的神经压迫症状,需要迅速解除压迫,二是需要手术才能获得肿瘤组织做病理检查,确定是什么肿瘤类型以决定下一步的治疗方案;手术原则是“在保护神经功能的情况下最大范围的切除”,也就是说,对位置比较表浅或位于额叶和颞叶这些相对次要位置的肿瘤要尽量扩大范围的切除,对位于脑组织深部或重要功能区(比如脑干和基底节区)的肿瘤只能尽量切除,甚至只能在立体定向和神经功能导航的情况下做病理活检;困难之处:脑肿瘤手术是难度最大的外科手术,一是因为胶质瘤沿着神经鞘膜浸润性生长,没有明确的边界,最多只能做到肉眼切除干净,很难病理学干净,二是开颅手术暴露有限,只能在一个有限的窟窿内用电凝刀和镊子就像掏耳屎一样一点一点地边止血边钳取,三是因为需要保护神经功能,大范围的切除可能导致严重的神经功能障碍,所以有“以空间换时间,以功能换生命”的说法,四是脑部手术并发症多且严重,很容易因为癫痫、出血、水肿、感染、脑脊液漏等导致昏迷不醒甚至死亡。鉴于以上原因,患者复发后想再次手术就更难了。 2.放射治疗:放射治疗和替莫唑胺同步化疗,和手术一样是胶质瘤的一线常规治疗,除了极少数低级别切除干净的一级的胶质瘤外,绝大多数二级和高级别的胶质瘤都需要术后放疗;生长在神经系统这种所谓慢反应组织中的胶质瘤尤其是高级别胶质瘤对放疗和化疗都欠敏感,但生长速度却很快,所以应在手术后尽早(尽早,一定是尽早)放疗和替莫唑胺同步化疗,共计6周时间(30次);放疗有普通放疗、三维适形放疗和调强适形放疗,无论从疗效还是副作用考虑,都应选择最先进的调强适形放疗,伽马刀只作为不耐受常规放疗患者或常规放疗后的补充治疗,而不是胶质瘤放疗的首选;除了个别弥漫性胶质瘤外,绝大多数胶质瘤都是在手术边缘2cm的范围内复发,NCCN治疗指南要求高级别胶质瘤的放疗剂量和范围为:术腔GTVtb和影像学可见的瘤体GTVp外1~2cm或水肿区的CTV2为60GY,再外放1cm的CTV1为50GY;低级别胶质瘤以水肿区域GTV外1-2cm做为CTV,剂量为46-54GY。困难之处:一是胶质瘤不像其它肿瘤(生长越快对放疗越敏感),它生长快但对放疗却不敏感,所以要尽量手术切除干净后放疗比较好,否则需要更高的放疗剂量,二是正常脑组织对放疗的耐受性有限,50GY就有可能导致功能受影响,超过60GY可能坏死形成空洞,也就相当于手术切除了,很多位置是不敢太高剂量照射的。总的来说,高的放疗剂量能获得高的肿瘤控制率,但也会增加功能损伤的可能,这需要得到病人和家人的充分理解。总的来说,放疗剂量高,就能得到高的肿瘤控制率,但相应的是副作用也会增多,医生需要根据肿瘤位置来确定放疗范围和剂量,权衡利弊:三是放疗的副作用是累积性的,绝大多素患者不宜做同一部位的再次放疗。 3.化疗:化疗包括放疗期间的同步替莫唑胺化疗和同期放化疗之后6个周期的替莫唑胺单药化疗,也是一线的常规治疗。鉴于手术和放疗的局限性,再次手术和再次放疗的机会都不大可能,患者不可避免地需要接受化疗;化疗药物的选择主要考虑能不能通过血脑屏障,主要药物有铂类(顺铂,卡铂)、氮芥类和亚硝脲类(甲基卞肼,ACNU,BCNU,CCNU)、植物碱类(长春新碱、VP16、VM26、去水卫矛醇)、代谢类(甲氨蝶呤)等,这些静脉化疗药物总体来说效果差且对血象影响大,只有1-2个月的治疗贡献,目前指南推荐的主要是替莫唑胺(TMZ),TMZ口服吸收良好,耐受性好,又能较好地通过血脑屏障。化疗主要应用于以下情况:放疗期间TMZ的同步化疗(75mg/㎡体表面积),放疗后连续6个疗程的TMZ单药化疗(200mg/㎡体表面积),基因检测有IDH突变、1p19q双缺失MGMT甲基化的患者(分子病理典型的少突胶质瘤,预计对化疗敏感)可考虑先用PCV方案或者TMZ化疗,病情进展后再考虑放疗,不能耐受手术和放疗的老年患者也适合用TMZ单药化疗,以及复发后不宜再次手术再次放疗患者的长疗程或高剂量治疗。困难之处:一是胶质瘤对放化疗欠敏感,二是因为血脑屏障的原因,化疗药物通过血脑屏障有限,最好的TMZ也只能有30%多,限制了化疗药物的疗效。ACT001是从小白菊中提取的植物类抗肿瘤药物,口服吸收良好,脑脊液中的浓度能达到血药浓度的1.8倍,是很有前途的脑肿瘤化疗药物,目前正在进行临床试验。 同步放化疗完成后休息2周以上继续行528方案的替膜唑安化疗(每28天一疗程、每疗程5天的替莫唑胺化疗,每天剂量为200mg/㎡体表面积),共计6个疗程,有残留等特殊情况需要9~12个周期的长疗程治疗,或应用其它的静脉化疗方案;对不是原发于脑的脑转移患者还需继续体部的全身治疗。 替莫唑胺口服方法:早上、下午或者晚上空腹时(饭后4小时以上)吃止吐药(格拉司琼或昂丹司琼胶囊)和胃药(奥美拉唑),半小时再吃替膜唑胺片,再过一小时后吃东西。 (以上的手术、手术后同步放化疗、放疗后6个疗程的替膜唑安治疗都属于一线治疗,也就是常规的疗效可靠的治疗。但是,高级别胶质瘤的复发是必然的,只是时间早晚的问题,复发的位置都在术腔边缘,少数为颅内的远隔部位或脑脊液播散,极少出现颅外转移。复发进展后的治疗属于二线治疗,治疗办法因人而异、疗效也未必确切。治疗办法包括:位置合适的可以考虑再次手术;未做过放疗或者距离上次放疗时间比较长、位置合适、病灶又不太大的可以再次放疗;未曾用过替膜唑安或者预计对替膜唑安还是敏感的病理类型可以继续用替膜唑安化疗,甚至用剂量密度方案;预计对替膜唑安不敏感的一般情况又比较好的患者也可以选择含铂类、长春新碱、vp16或者CCNU药物的静脉化疗;大多数病人比较现实和疗效比较可靠的是抗肿瘤血管生成治疗;有条件尤其是经济条件好的可以选择TTF电场治疗;根据基因检测,少数患者可以适合靶向药物治疗或者免疫治疗;经病理切片检测有合适抗原抗体的可以做CAR_T免疫治疗;一般情况差或者高龄患者又不没有以上的选项,只适合对症支持治疗,包括脱水、皮质激素等) 4.抗血管生成治疗:抗肿瘤血管生成靶向药物是手术和放化疗失败后的最现实有效的二线治疗。除了少数级别低、位置浅表和位于相对次要位置的胶质瘤外,绝大多数患者接受常规的手术—同步放化疗—替莫唑胺化疗后都会出现肿瘤未控或者复发,在不能再次手术再次放疗、化疗效果不好的情况下需要应用二线治疗药物,包括更换化疗药物和使用抗肿瘤血管生成抑制剂(贝伐单抗、恩度、泰欣生、舒尼替尼、索拉非尼、阿帕替尼、安罗替尼、乐伐替尼、帕唑替尼、依鲁替尼、瑞格菲尼等)。贝伐单抗(安维丁,AVASTIN)精准靶向抑制VEGF,抑制肿瘤血管生成,减少肿瘤营养,持续控制肿瘤的生长;同时,血管内皮被抑制后外渗减少,对脑水肿和放射性脑病有非常好的控制作用,其脱水效率是甘露醇和地塞米松的4倍以上。每次用量7.5mg/kg,每21天重复一次。困难之处:应用一段时间后会逐渐耐药,另外会增加出血的风险和延迟伤口愈合。 5.电磁场治疗: 电场治疗也是常用的二线治疗,甚至是老年人胶质母细胞瘤的一线治疗手段。NovoTTF-100A型便携式肿瘤治疗仪通过一个便携式无创医疗器械实施,供患者连续佩戴覆盖头部的电极板使用,具有副作用少(主要是头皮过敏)、佩戴方便,但价格昂贵等特点。体外和体内研究显示,TTF治疗仪电场治疗仪在肿瘤内部形成低强度的交流电场,该电场对充电的细胞部件进行物理施力,阻止肿瘤细胞有丝分裂,从而促使癌细胞死亡。四级胶母细胞瘤佩戴该治疗仪平均生存期提高6.3个月(从14.6个月到20.9个月),2年OS为42%对比29%),5年OS为10%对比5%。困难之处:价格昂贵,要求每天佩戴17小时以上。 6.分子靶向药物治疗:在目前的胶质瘤诊治中都建议做全面的分子病理检测,最好是全外显子检测,一是有利于肿瘤分型和分级,二是判断预后,三是预测化疗药物的敏感性,四是寻找合适的分子靶向药物,但只有少数病人能找到合适的靶向药物,如针对VEGFR突变的血管靶向药物、针对BRAF V600E突变的维罗菲尼、针对mTOR通路的依维莫司和雷帕霉素、针对EGFR的阿法替尼、针对STAT3位点的依鲁替尼等。困难之处:只有少数患者能检测到,而且应用一段时间后会形成耐药。 7.免疫治疗:中枢神经系统在免疫方面存在以下特点:淋巴组织及淋巴回流系统的匮乏;脑内抗原递呈细胞的缺失;正常脑组织主要组织相容性复合体(major histocompatibility complex,MHC)抗原表达不可检测;血脑屏障的存在,阻挡了抗体和淋巴细胞的渗透所以,脑肿瘤是缺乏免疫的'冷肿瘤';目前胶质瘤的免疫治疗还是探索性的,没有大宗的临床研究证实其有效性,主要项目包括:树突状细胞疫苗(DC)、肿瘤浸润性淋巴细胞(TIL)、CAR-T细胞、PD-1和PD-L1免疫药物等。困难之处:一是必须经过检测和筛选才能知道适合做哪种免疫治疗,只有部分病人适合,二是疗效不确切。 8.OMAYA囊治疗:对于一些囊腔封闭的胶质瘤患者,在瘤腔内留置OMAYA储液囊,相当于埋藏在皮下的输液港,可以随时向囊腔内注射化疗药物、放射性同位素、以及免疫细胞药物等,具有使用方便、没有全身毒性等特点。前提是:囊腔必须是封闭的。 9.中药方剂。我们的部分胶质母细胞瘤病人采用中药方剂也取得了不错的效果,但缺乏大宗的循证医学证据,在常规治疗无效的情况下,任然是一种治疗选择和尝试。
 张俊德 主任医师 南方医科大学珠江医院 放疗科2.7万人已读
张俊德 主任医师 南方医科大学珠江医院 放疗科2.7万人已读
问诊记录 查看全部
- 肺癌腰椎转移 腰腿不适症状十多年;
近一年症状加重,右胯骨及右膝盖疼痛无力... 请教大夫:
患者在放疗前的白细胞和血小板都低,需要用药治疗吗?总交流次数10已给处置建议
- 脑干胶质瘤 2020.4.7确诊在珠江医院做了部分切除,同年九总交流次数6已给处置建议
- 胶质瘤 右侧额叶占位术后改变,残腔及周围胶质增生较前相仿,总交流次数2已给处置建议
- 肺腺癌脑转移 奥西替尼吃了9个月,肺癌脑转移, 是否进行放疗?还能等多长时间再放疗?总交流次数7已给处置建议
- 胶质母细胞瘤(WHOIV级) 胶质瘤年轻患者如何治疗,提高生存率?总交流次数4已给处置建议