科室医生 查看全部
科普·直播义诊专区 查看全部
- 精选 前列腺癌放射治疗策略与进展(综述)
作者:亓昕李洪振作者单位:北京大学第一医院放射治疗科随着调强放射治疗、影像引导放射治疗、立体定向放射治疗、质子放射治疗等放射治疗技术的不断发展与进步,前列腺癌的放射治疗进入了一个全新的精准放射治疗时代。精准放射治疗可在有效杀死肿瘤细胞的同时,尽量避免或减少对肿瘤周围正常组织的损伤,从可显著提高前列腺癌放射治疗的临床疗效,并可减少不良反应的发生。本文将对不同时期前列腺癌的放射治疗策略与进展进行总结,主要包括非转移性前列腺癌的根治性放射治疗、根治性前列腺切除术后的辅助放射治疗或挽救性放射治疗、转移性前列腺癌原发灶和转移灶的放射治疗。1、非转移性前列腺癌的根治性放射治疗1.1提高放射治疗剂量对生存的影响MRCRT01随机对照试验结果表明,提高放射治疗剂量可以显著改善非转移性前列腺癌患者的无生化失败生存率[1]。目前对于局限期的低中危前列腺癌患者,推荐给予75.6~79.2Gy的常规分割根治剂量:对于高危病例,建议给予81Gy以上的常规分割根治剂量[2]。需要强调的是,如此高的放射治疗剂量必须建立在优质质量控制的前提下,如采用每日影像引导放射治疗可明显减少不良反应,提高临床疗效。一项来自21个中心的Ⅲ期随机对照试验结果显示,与采用每周影像引导放射治疗比较,采用每日影像引导放射治疗可显著减少前列腺癌患者3级以上晚期直肠不良反应的发生,同时可改善前列腺癌患者的无生化失败生存率[3]。1.2剂量分割模式多项研究均证实,与常规分割根治剂量(1.8~2Gy/次)比较,中等分割根治剂量(2.4~4Gy/次)模式可将前列腺癌患者的放射治疗总时长从过去的8周缩减至3~5周,且临床疗效更佳,患者依从性更好[4-8]。NOSSITER等[9]的研究报道,与前列腺癌常规分割根治剂量比较,中等分割根治剂量的治疗失败率更低,安全性方面两者无显著差异。因此,目前国际主流指南均推荐,非转移性前列腺癌的根治性放射治疗可以选择中等分割根治剂量替代常规分割根治剂量,可供参考的剂量分割模式有:3Gy×20次、2.7Gy×26次、2.5Gy×28次以及2.8Gy×25次。与常规分割比较,大分割放射治疗(单次剂量>5Gy,立体定向消融放射治疗)能否提高前列腺癌患者的总生存率和肿瘤特异性生存率仍需要进一步的研究来证实,但大分割放射治疗可使患者消化系统和泌尿系统的晚期不良反应发生率显著升高[10]。因此,现阶段推荐将大分割放射治疗纳入临床研究的范畴更为安全、合理。近年来,为降低大分割放射治疗可能带来的直肠不良反应发生率,国内外均尝试采用在直肠前壁和前列腺之间注射凝胶间隔物等新技术来解决,间隔物可以显著减少直肠高剂量照射区域[11]。1.3局部加量:由于前列腺癌是多灶性病变,在影像学上很难发现所有卫星病灶,所以过去都是将前列腺整体进行高剂量放射治疗。已有研究显示,放射治疗后前列腺穿刺活检阳性的前列腺癌患者的预后明显差于前列腺穿刺活检阴性的前列腺癌患者,复发部位一般位于磁共振成像可见的结节处[12]。更为精准的前列腺特异性膜抗原正电子发射断层成像(positronemissiontomography,PET)/计算机断层扫描(computedtomography,CT)和多参数磁共振成像使得对前列腺癌临床显著病灶进行局部加量成为可能。局部加量的方式有常规分割序贯近距离加量、常规分割同步加量以及立体定向消融放射治疗同步加量等。FLAME研究显示,采用常规分割同步加量模式可显著降低局限性中高危前列腺癌患者的局部复发风险和远传转移风险[13]。目前,如何精准定义局部加量区是研究的热点和重点,已有研究显示,采用前列腺特异性膜抗原PET/CT联合多参数磁共振成像定义局部加量区的敏感度和特异度分别为91%和84%[14]。因此,推荐采用前列腺特异性膜抗原PET/CT联合多参数磁共振成像来定位前列腺癌病灶。1.4联合治疗ProtecT研究发现,局限期极低危、低危以及预后良好的中危前列腺癌患者采用单纯根治性放射治疗可以获得与根治性前列腺切除术相同的临床疗效,无论采取手术还是单纯放射治疗,这部分患者的肿瘤特异性生存率均为99%,因此这类患者采用放射治疗时无须联合雄激素剥夺疗法[15]。对于预后不良的中危前列腺癌患者,与单纯放射治疗比较,采用同步短程雄激素剥夺疗法+放射治疗可以显著降低其生化失败率和疾病特异性死亡率[16]。对于高危、极高危、局部进展期的前列腺癌患者,EORTC22863研究结果显示,与单纯放射治疗比较,长程雄激素剥夺疗法+放射治疗可显著改善患者的10年总生存率(39.8%比58.1%,HR=0.6,P=0.0004)[17]。1.5高恶性度前列腺癌的综合治疗:高恶性度前列腺癌的转移风险较高,因此,常需联合其他全身治疗手段,化疗可能是有效方法。RTOG0521研究结果显示,在雄激素剥夺疗法+放射治疗放疗的基础上辅助多西他赛化疗,可以改善高恶性度前列腺癌患者的4年总生存率(89%比93%,HR=0.69,P=0.034)[18]。2、根治性前列腺切除术后的放射治疗2.1放射治疗时机:辅助放射治疗是指对具有病理高危因素(pT3-4、切缘阳性、Gleason评分为8~10分)的前列腺癌根治性前列腺切除术后患者,待术后尿失禁缓解后进行放射治疗。挽救性放射治疗是指对术后生化失败的前列腺癌患者(术后前列腺特异性抗原(prostatespecifcantigen,PSA)水平未降至正常水平或降低后又升高,超过0.1ug/L进行放射治疗。关于术后辅助放射治疗和挽救性放射治疗的争论从未停止,率先获得高级别证据支持的是辅助放射治疗。4项随机对照试验(SWOG8794研究、EORTC22911研究、ARO9602研究、FinnProstateGroup研究)评估了术后辅助放射治疗的价值,结果显示,对术后具有病理高危因素的前列腺癌患者,辅助放射治疗可降低53%的生化复发风险[19-22]。但需要注意的是,在这4项随机对照试验中,只有ARO9602研究纳入患者的PSA是处于测不出水平,其他3项研究中有1/3患者的PSA水平超过了0.2ng/ml,因而无法解释清楚是挽救性放射治疗还是辅助放射治疗所起的作用。为了弄清挽救性放射治疗是否可以替代辅助放射治疗,3项随机对照试验(RADICALS-RT研究、RAVES研究、GETUG-AFU17研究)比较了辅助放射治疗和挽救性放射治疗的临床疗效[23-25]。截至目前这3项随机对照试验只公布了无生化失败生存率的结果,辅助放射治疗和挽救性放射治疗比较无显著差异。值得注意的是,这3项随机对照试验选择的患者均为术后进展风险较低的前列腺癌患者(pT3R0或pT2R1),其本身可能无法从辅助放射治疗中显著获益。目前,国内更多前列腺癌患者具有更高的Gleason评分和切缘阳性率,这部分人群更需要尽早进行辅助放射治疗。因此,仍推荐对术后具有高危病理因素者的前列腺癌患者行辅助放射治疗,对术后无病理高危因素者但PSA未降至正常水平或生化复发的前列腺癌患者行挽救性放射治疗。2.2复发高危因素和基因分型:术后国际泌尿病理协会分级≥3级、包膜受侵、精囊受侵、切缘阳性是前列腺癌患者术后复发的高危因素,术后5年复发率高达50%。对于术后淋巴结转移的前列腺癌患者,淋巴结清扫数目、转移淋巴结体积、转移淋巴结包膜受侵是术后早期复发的预测因子,淋巴结密度(阳性淋巴结/清扫淋巴结)>20%是预后不良的独立影响因素。近年来,生物标志物的迅速发展助力前列腺癌术后患者的精准分层,其中研究较为深入的是Decipher基因检测,可以预测前列腺癌术后患者未来的疾病进展风险。2.3前列腺特异性膜抗原正电子发射断层成像对术后放射治疗的影响PERERA等[26]的研究纳入4790例前列腺癌患者,结果显示,PSA<0.2ug/L时,前列腺特异性膜抗原PET的病灶检出率为33%:PSA为0.2~0.5ug/L时,其病灶检出率为45%。AFSHAR-OROMIEH等[27]的研究纳入2533例前列腺癌患者,结果显示,PSA<0.2ug/L时,前列腺特异性膜抗原PET/CT的病灶检出率为43%,PSA为0.2~0.5ug/L时,其病灶检出率为58%,PSA为0.5~1ug/L时,其病灶检出率为72%。前列腺特异性膜抗原PET的结果可影响前列腺癌患者后续治疗方案的制订,影响方式主要包括:改变放射治疗计划(增加放射治疗范围和提高放射治疗剂量),增加全身用药,如发现寡转移,可行转移部位放疗,如发现多发转移,需要联合新型内分泌治疗药物或化疗。但这种治疗方案的改变是否可提高前列腺癌患者的总生存期,目前尚无高级别的证据支持。另外对于术后即刻开始内分泌治疗的患者,无需进行前列腺特异性膜抗原PET检查。2.4术后放射治疗剂量:美国国家综合癌症网络指南推荐前列腺癌的术后放射治疗剂量为64~72Gy[28],范围较为宽泛,尚缺乏更为个体化的推荐方案。目前国际上报道了2项关于前列腺癌术后放射治疗剂量的随机对照试验,分别是北京大学第一医院的研究[29]和欧洲的SAKK09/10研究[30]。北京大学第一医院的研究率先公布结果,中位随访4.2年后,与传统剂量(66Gy)比较,强化剂量(72Gy)放射治疗后患者的生存结果和不良反应均无显著差异,但是在Gleason评分≥8分的亚组前列腺癌患者中,72Gy可使患者获得优于66Gy的无进展生存期(P=0.0498)[29]。2021年SAKK09/10研究公布结果,其生存结果与北京大学第一医院的研究相似,但不良反应发生率更高[30]。目前北京大学第一医院的研究的中位随访时间已经达到7.5年,更长的随访时间进一步体现出了强化剂量(72Gy)对Gleason评分≥8分前列腺癌患者的生存获益(P=0.0118),进一步的亚组分析结果显示,术后多灶切缘阳性的前列腺癌也需要更高的放射治疗剂量[29]。2.5联合治疗对于术后仅有病理高危因素、无生化复发的前列腺癌患者,目前尚无辅助放射治疗同时联合内分泌治疗的临床证据。但是对于生化失败的前列腺癌患者,特别是PSA倍增时间短、恶性度高的前列腺癌患者,建议辅助内分泌治疗6个月左右。对于术后PSA倍增时间长、PSA水平低的患者,可首先进行挽救性放射治疗,若放射治疗后PSA水平下降,无需再进行内分泌治疗[31]。另外分子分型也可指导术后内分泌治疗策略,若Decipher评分>0.6分,建议行放射治疗联合内分泌治疗。3、转移性前列腺癌放射治疗根据放射生物学理论,前列腺癌的a/β值较低,更适合大分割立体定向消融放射治疗模式,对单发淋巴结转移、骨转移、内脏转移的前列腺癌患者均可采用立体定向消融放射治疗模式。对于无症状的转移性前列腺癌,是否能通过放射治疗达到减瘤,并进一步延长患者的生存期值得进一步讨论。需要先甄别能够从局部治疗中获益的前列腺癌人群,转移性前列腺癌常见分类方式包括按照肿瘤负荷(高瘤负荷、低瘤负荷)分类和按照转移时机(同时性、异时性)分类。其中低瘤负荷,又称寡转移,目前常定义为转移灶数目≤5处,是一种介于无转移和广泛转移的中间状态,有可能通过强化局部治疗,获得治愈机会。2018年以前,国际主流指南(美国国家综合癌症网络指南、美国泌尿学会指南、欧洲泌尿学会指南)对转移性前列腺癌的推荐治疗方式仅有以雄激素剥夺疗法为基石的药物治疗。2019年,随着2项前瞻性随机对照试验研究(HORRAD研究和STAMPEDE研究)结果的发布,原发灶放射治疗被证实可以延长初诊为寡转移激素敏感性前列腺癌患者的总生存期,因此转移性前列腺癌原发灶放射治疗成为了指南中的1类推荐,这是转移性前列腺癌治疗原则的一个重要改变[32-33]。STAMPEDE研究中瘤负荷是采用CHAARTED研究中的定义,高瘤负荷的标准是4处及以上骨转移灶+1处及以上转移位置不在椎体/骨盆,或有内脏转移,需要注意的是,CHAARTED研究中所用的影像学检查手段为传统影像学检查手段(CT和骨扫描)。新一代影像学检查手段,如前列腺特异性膜抗原PET发现的转移灶数目是否还能沿用既往的寡转移定义,仍是一个值得商榷的问题。寡复发,又称异时性寡转移,此类患者在根治性前列腺切除术或放射治疗后,原发灶得以控制,但复查过程中发现PSA水平升高,进一步行影像学检查发现转移病灶。目前,前列腺特异性膜抗原PET检查广泛应用于根治性前列腺切除术后生化失败的前列腺癌患者中,其在PSA较低水平时即可检查出临床病灶。2项前瞻性随机对照试验(STOMP研究和ORIOLE研究)结果显示,转移灶放射治疗能够延长寡复发患者的无进展生存期,推迟开始内分泌治疗的时间[34-35]。目前,关于同时性和异时性前列腺癌患者内分泌治疗的方案和持续时间尚无定论。目前指南只推荐原发灶放射治疗,从理论上讲,只有所有病灶都接受了治疗,才能阻止原发灶向转移灶、转移灶向转移灶的播散,从而实现最大程度的减瘤,让寡转移患者得以向局限疾病的逆转,并可能达到根治的目的。因此,在临床诊疗实践中,北京大学第一医院采用了原发灶+转移灶“全覆盖“的强化放射治疗模式,初步结果显示,对于寡转移前列腺癌患者,“全覆盖“放射治疗模式安全、有效,且激素敏感性前列腺癌患者的预后优于进展至激素抵抗性阶段再进行“全覆盖“放射治疗,因此推荐转移性前列腺癌患者尽早接受“全覆盖“放射治疗。总体来说,各个分期前列腺癌的放射治疗策略未来都会朝精准化、个体化方向发展,且还需要更多中国人群的研究数据来进一步指导临床实践。参考文献:略。(出处:中国医刊2023年第58卷第6期)
李洪振 主任医师 北京大学第一医院 放射治疗科433人已读 - 精选 前列腺癌放射治疗策略与进展(综述)
前列腺癌放射治疗策略与进展(综述)作者:亓昕李洪振作者单位:北京大学第一医院放射治疗科随着调强放射治疗、影像引导放射治疗、立体 定向放射治疗、质子放射治疗等放射治疗技术的不断发展与进步,前列腺癌的放射
亓昕 副主任医师 北京大学第一医院 放射治疗科3003人已读 - 精选 寡转移前列腺癌放疗的研究进展
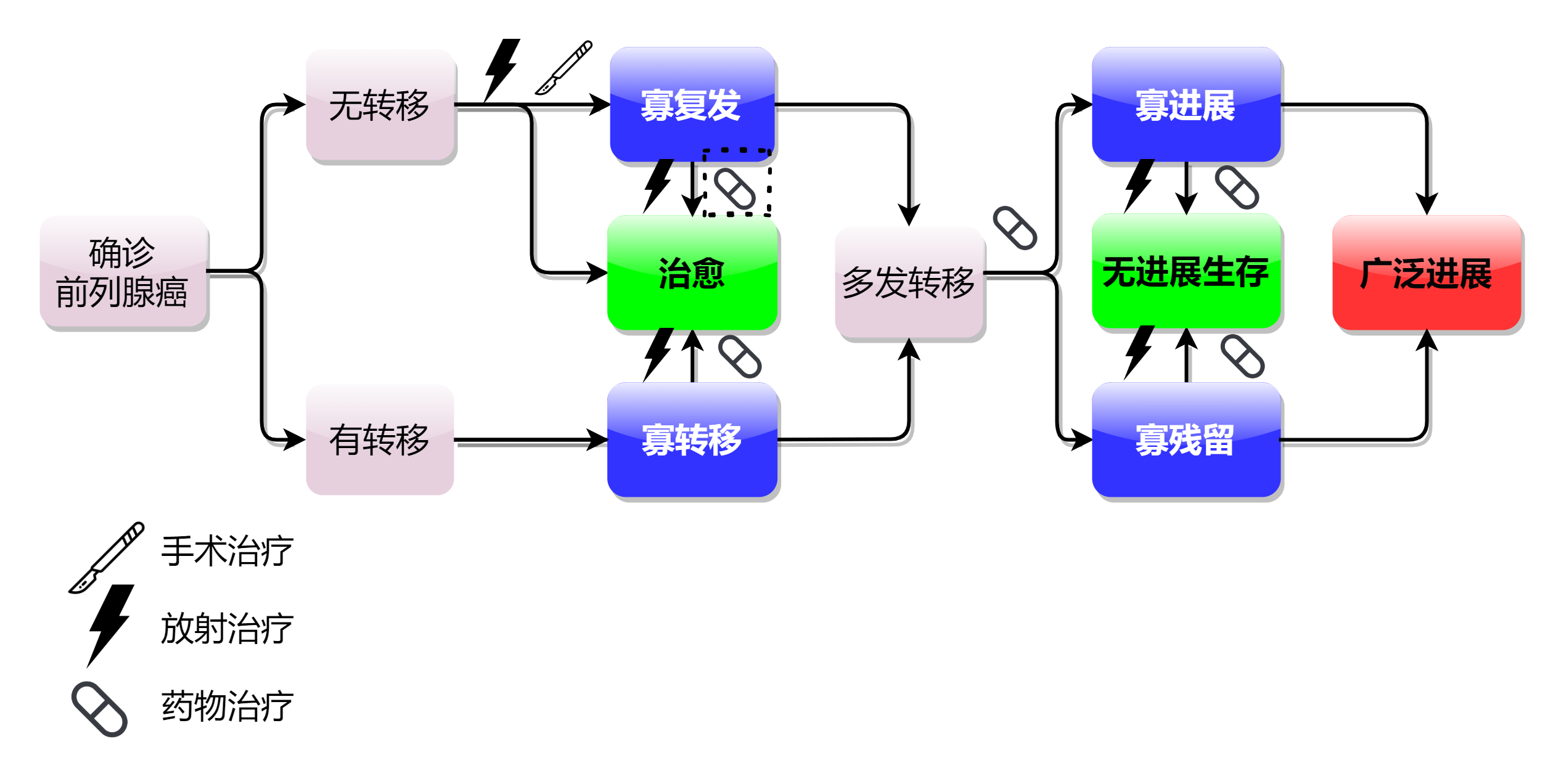
寡转移前列腺癌放疗的研究进展作者:亓昕、李洪振北京大学第一医院前列腺癌是男性泌尿生殖系统最常见的恶性肿瘤。据统计,2023年美国前列腺癌新发病例位居美国男性肿瘤第一位,死亡率位居第二位。我国的前列腺癌
 李洪振 主任医师 北京大学第一医院 放射治疗科581人已读
李洪振 主任医师 北京大学第一医院 放射治疗科581人已读
问诊记录 查看全部
- 左肾癌根治术后7个月 患者于2023年9月28日行根治性肾癌切除手术,手术过程切除... 想问问您我这个情况做放疗是最优选择吗?做的话有没有必要去北京做,排队的话得等多久总交流次数13已给处置建议
- 化疗2次后续治疗 化疗两次后,身体状态有些不好。心脏跳的快,血糖也不稳定 ... 是否建议停止化疗,换成放疗总交流次数15已给处置建议
- 肾癌骨转移 L4L5椎骨受侵犯 肾透明细胞癌 腹膜后转移 骨转移 2024-3-22日在本院骨科进行手术后
目前已进行三次放疗... 1-放疗三次后副反应过于大:恶心呕吐,排便困难
2-实在太难受可否间断一天总交流次数13已给处置建议
- 前列腺癌 目前患者无明显不适,仅乏力,有时咳嗽,无骨痛,但面色差。 ... 亓主任,6化已结束,6化前PSA0.259,确诊前35。
1.现在可以放疗吗?需要准备什么资料。
...总交流次数18已给处置建议
- 前列腺癌 18年因前列腺癌做了放疗治,前两天抽血,请主任帮看看结果,谢... 请主任帮看看结果总交流次数10已给处置建议
总访问量 1,141,992次
在线服务患者 1,843位
科普文章 18篇
领导风采













