医院介绍 查看全部
科普·直播义诊专区 查看全部
- 精选 甲状腺疾病患者,更容易感染新冠病毒吗?
冠疫情爆发之初,人类对于新冠病毒知之甚少,大多数的建议仅仅是基于过去的常识。随着世界各国史无前例的科研投入,关于新冠病毒相关的研究呈裂变式激增,不断刷新我们对新冠的认知。仅在美国Pubmed上检索,2020年1月至2021年12月26日,涉及新冠相关文献超过20万篇,其中涉及新冠与甲状腺相关的文献也多达517篇。新冠爆发至今已2周年,人类与新冠的鏖战还在继续。汇集这些最新的研究以解答甲状腺疾病与新冠相关的疑问,希望能对疫情之下甲状腺疾病患者有所帮助。PubMed是世界上最权威的医学文献数据库之一,可提供生物医学和健康科学领域文献免费搜索服务。互联网时代,医学文献不再是医生的专享,如果您想深入了解疾病相关知识,可登录网址https://pubmed.ncbi.nlm.nih.gov检索,让自己做一个不再盲从的患者,大胆与医生探讨你的病情和治疗方案。■感染新冠病毒后,是否会导致甲状腺疾病风险?与100年前西班牙流感相比,新冠传播速度更快、且致死性更强。初期人们认为新冠病毒只是入侵呼吸系统,导致严重急性呼吸系统综合征。但是,随后的临床观察发现,除外肺部受损,还可以导致血管、心脏、肾、胃肠道、肝脏、胰腺、神经系统、眼及皮肤等并发症。尽管采用了当今最先进的医疗技术,由于多系统、多器官的受累和叠加仍然导致新冠感染者存在较高的死亡率(约2%)。目前的研究表明新冠病毒利用血管紧张素转换酶2(ACE2)受体进入细胞。由于ACE2在肺、血管、心脏、肾脏、胃肠等组织和器官广泛分布,因而这些组织和器官更容易受到新冠病毒的攻击。随着更广泛深入的研究,还发现甲状腺组织中也存在ACE2表达。因而,甲状腺同样也可能受到新冠病毒的直接攻击而导致甲状腺滤泡细胞破坏。另外,甲状腺还可能间接受到因其他组织和器官受到新冠病毒攻击而诱发的细胞因子风暴的影响。因此,从理论上推测,感染新冠病毒后可能导致甲状腺疾病风险增加。源自文献:MuruganAK,AlzahraniAS.SARS-CoV-2:EmergingRoleinthePathogenesisofVariousThyroidDiseases.JInflammRes.2021Nov24;14:6191-6221.Lui等人报道新冠感染住院患者中约15%发生甲状腺功能异常。另外,有文献报道感染新冠后出现桥本甲状腺炎、Graves甲亢、Graves眼病及亚急性甲状腺炎等甲状腺疾病的案例,其中以亚急性甲状腺炎案例数量最多。但是,美国约翰·霍普金斯大学大数据分析未能得出新冠感染者存在较高的甲状腺疾病发生率。■甲状腺疾病患者,更容易感染新冠吗?虽然甲状腺组织中存在ACE2表达,似乎甲状腺疾病患者可能更容易感染新冠病毒。但是,真实世界的情况并非如此:●没有证据表明未能有效控制的甲亢患者更容易感染新冠,也没有数据表明抗甲状腺药物、或碘-131治疗、或手术会增加甲亢患者新冠感染风险。但是,如果因药物副作用导致白细胞减少,可能导致对新冠易感或新冠感染后病情更严重。另外,因Graves眼病(突眼)服用类固醇激素或其他免疫抑制药物治疗的患者,由于处于免疫力下降的时期,因而也易感染新冠。●一些研究显示癌症患者更容易感染新冠,而且感染新冠后也更容易导致严重的病情。来自武汉的数据显示:伴有癌症的新冠感染者因新冠相关死亡率较没有伴癌症的新冠感染者高10倍。但是,针对分化型甲状腺癌患者感染新冠后数据分析,并没有对预后结果产生不利影响,即使术后碘-131治疗也没有导致新冠相关不良影响。这可能归因于分化型甲状腺癌较为惰性,且绝大多数患者预后良好。●2021年8月发表的一篇韩国全国性队列研究表明,与普通人群相比,并没有显示出甲状腺疾病患者更容易感染新冠。■感染新冠病毒后,是否会导致甲状腺疾病患者复发或加重?病毒感染常被认为是参与自身免疫性甲状腺疾病发病的主要环境因素。依据既往的经验推演,新冠感染导致的炎性反应可能诱发免疫级联反应,从而使Graves甲亢、Graves眼病及桥本氏甲状腺炎等自身免疫性甲状腺疾病复发或加重。 虽然一些文献先后报道了感染新冠后甲亢复发和加重。但是,尚不清楚是时间上的巧合,还是疫情所致精神因素影响,今后还需要进一步的研究来阐释其中的发病机制。■接种新冠疫苗,是否会导致甲状腺疾病风险?自2011年Shoenfeld首次提出佐剂诱导自身免疫/炎症综合征(ASIA)以来,有许多关于为了提高疫苗接种的免疫应答而添加的佐剂导致ASIA的报道和研究,其中也包括佐剂诱导甲状腺疾病。例如接种流感病毒疫苗、人乳头瘤病毒(HPV)疫苗后新发甲状腺疾病的报道。大规模新冠疫苗接种后,也出现了可能与ASIA相关的案例报道,其中涉及甲状腺相关疾病报道最多的是亚急性甲状腺炎,其他还有Graves甲亢、无痛性甲状腺炎、桥本氏甲状腺炎等。 除外疫苗中的佐剂,疫苗本身也可能导致自身免疫性甲状腺疾病。因此,从理论上讲,接种新冠疫苗可能增加易感人群发生甲状腺疾病风险。■接种新冠疫苗,是否会导致原有甲状腺疾病复发或加重?对于患有或曾患有自身免疫性甲状腺疾病的病人,更可能受到疫苗中的佐剂及疫苗本身导致的自身免疫被重新激活或加剧,从而导致甲状腺疾病复发或加重。无论是新冠的灭活疫苗、或腺病毒载体疫苗、或mRNA疫苗,已有相关案例被报道,接种疫苗不久后出现Graves甲亢和Graves眼病的复发或加重。 但是,对于甲状腺癌患者,是否导致疾病复发或加重?目前还没有相关案例报告。美国食品和药物管理局(FDA)批准上市的两种疫苗临床试验结果显示,恶性肿瘤患者疫苗接种的安全性与普通健康人一样。■面对持续的疫情,甲状腺疾病患者该如何应对?理论上感染新冠或接种疫苗后甲状腺疾病患者存在复发或加重的风险。但是,目前的研究尚未证实新冠疫苗接种与自身免疫性疾病的发展之间存在因果关系。相较于全球范围的新冠感染者和大规模新冠接种人群而言,零星的个案报道说明这种风险仍然极低。相反,接种新冠疫苗所带来的好处显而易见。 2021年11月一篇文献综述报道:接种1剂疫苗后预防新冠感染的有效率为28%-54%,接种2剂疫苗后可显著提高至81%-89%。即便感染新冠,接种1剂疫苗后新冠死亡率可降低15%-91%,接种2剂疫苗后可显著降低至92%-98%。 目前新冠疫苗接种是抗击疫情最有效的预防措施,与接种疫苗所带来的益处相比,微不足道的不良反应是完全可以接受的。面对持续的疫情,甲状腺疾病患者该如何应对?现有的文献及英国、巴西、欧洲、韩国等甲状腺/内分泌协会给出了建议:●甲状腺癌、桥本氏甲状腺炎、Graves甲亢及甲减等甲状腺疾病不是新冠疫苗接种的禁忌证。●甲状腺疾病患者应按照与普通人群一样的标准接种新冠疫苗。●尽快控制甲亢,以防止因感染新冠而诱发严重并发症(如甲状腺危象)。●Graves眼病(突眼)活动期,建议暂时延后新冠疫苗接种。●Graves眼病(突眼)激素治疗期间,应更加严格的做好个人防疫措施。●Graves甲亢抗甲状腺药物治疗期间,如因药物副作用发生白血病减少,应及时停药。跨界科普,如有错误,敬请指正!参考文献:[1]BragazziNL,HejlyA,WatadA,etal.ASIAsyndromeandendocrineautoimmunedisorders.BestPractResClinEndocrinolMetabol2020;34(1):101412.[2]BTA/SFEstatementregardingissuesspecifictothyroiddysfunctionduringtheCOVID-19pandemic.[3]COVID-19dataportal,CenterforSystemsScienceandEngineering,TheJohnsHopkinsUniversity,BaltimoreMDUSA.[4]DasL,BhadadaSK,SoodA.Post-COVID-vaccineautoimmune/inflammatorysyndromeinresponsetoadjuvants(ASIAsyndrome)manifestingassubacutethyroiditis.JEndocrinolInvest.2021Sep28;1-3.[5]DeligiorgiMV,SiasosGVakkasL,etal.ChartingtheUnknownAssociationofCOVID-19withThyroidCancer,FocusingonDifferentiatedThyroidCancer:ACallforCaution.Cancers(Basel).2021Nov18;13(22):5785.[6]DesailloudR,HoberD.Virusesandthyroiditis:anupdate.VirolJ.2009Jan12;6:5.[7]diFilippoL,CastellinoL,GiustinaA.OccurrenceandresponsetotreatmentofGraves'diseaseafterCOVIDvaccinationintwomalepatients.Endocrine.2021Nov2;1-3.[8]FeghaliK,AtallahJ,NormanC.ManifestationsofthyroiddiseasepostCOVID-19illness:ReportofHashimotothyroiditis,Graves'disease,andsubacutethyroiditis.JClinTranslEndocrinolCaseRep.2021Dec;22:100094.[9]GiustinaA,MarazuelaM,ReinckeM,etal.Oneyearofthepandemic-howEuropeanendocrinologistsrespondedtothecrisis:astatementfromtheEuropeanSocietyofEndocrinology.EurJEndocrinol.2021Jul5;185(2):C1-C7.[10]Gorini F,BianchiF,IervasiG.COVID-19andThyroid:ProgressandProspects.IntJEnvironResPublicHealth.2020Sep11;17(18):6630.[11]GuptaA,MadhavanMV,SehgalK,etal.ExtrapulmonarymanifestationsofCOVID-19.NatMed.2020Jul;26(7):1017-1032.[12]HarrisA,MushrefMA.Graves'ThyrotoxicosisFollowingSARS-CoV-2Infection.AACEClinCaseRep.Jan-Feb2021;7(1):14-16.[13]Jiménez-BlancoS,Pla-PerisB,MarazuelaM.COVID-19:acauseofrecurrentGraves'hyperthyroidism?JEndocrinolInvest.2021Feb;44(2):387-388.[14]KimSY,YooDM,MinCY,etal.TheEffectsofPreviousThyroidDiseaseontheSusceptibilityto,Morbidityof,andMortalityDuetoCOVID-19:ANationwideCohortStudyinSouthKorea.JClinMed.2021Aug11;10(16):3522.[15]KuCR,JungKY,AhnCH,etal.COVID-19VaccinationforEndocrinePatients:APositionStatementfromtheKoreanEndocrineSociety.EndocrinolMetab(Seoul).2021Aug;36(4):757-765.[16]LanzollaG,MarcocciC,MarinòM.Graves'diseaseandGraves'orbitopathyfollowingCOVID-19.JEndocrinolInvest.2021Sep;44(9):2011-2012.[17]LeeKA,KimYJ,JinHY.ThyrotoxicosisafterCOVID-19vaccination:sevencasereportsandaliteraturereview.Endocrine.2021Dec;74(3):470-472.[18]LugerA,GiustinaA,PeetersR.EuropeanSocietyofEndocrinology(ESE)’sstatementconcerningCOVID19vaccination:‘followthesamerecommendationsforpatientswithstableendocrinedisordersasforthegeneralpopulation’2021[Internet]Bristol:EuropeanSocietyofEndocrinology;2021.[19]LuiDTW,LeeCH,ChowWS,etal.ThyroidDysfunctioninRelationtoImmuneProfile,DiseaseStatus,andOutcomein191PatientswithCOVID-19.JClinEndocrinolMetab.2021Jan23;106(2):e926-e935.[20]MartinsJRM,VillagelinDGP,CarvalhoGA,etal.ManagementofthyroiddisordersduringtheCOVID-19outbreak:apositionstatementfromtheThyroidDepartmentoftheBrazilianSocietyofEndocrinologyandMetabolism(SBEM).ArchEndocrinolMetab.2021Nov3;65(3):368-375.[21]Mateu-SalatM,UrgellE,ChicoA.SARS-COV-2asatriggerforautoimmunedisease:reportoftwocasesofGraves'diseaseafterCOVID-19.JEndocrinolInvest.2020Oct;43(10):1527-1528.[22]MontebelloA.RecurrentGraves'diseasepostSARS-CoV-2infection.BMJCaseRep.2021Aug6;14(8):e244714.[23]MuruganAK,AlzahraniAS.SARS-CoV-2playsapivotalroleininducinghyperthyroidismofGraves'disease.Endocrine.2021Aug;73(2):243-254.[24]MuruganAK,AlzahraniAS.SARS-CoV-2:EmergingRoleinthePathogenesisofVariousThyroidDiseases.JInflammRes.2021Nov24;14:6191-6221.[25]PiermanG,DelgrangeE,JonasC.RecurrenceofGraves'Disease(aTh1-typeCytokineDisease)FollowingSARS-CoV-2mRNAVaccineAdministration:ASimpleCoincidence?EurJCaseRepInternMed.2021Sep2;8(9):002807.[26]PizzocaroA,ColomboP,VenaW,etal.OutcomeofSars-COV-2-relatedthyrotoxicosisinsurvivorsofCovid-19:aprospectivestudy.Endocrine.2021Aug;73(2):255-260.[27]Puig-DomingoM,MarazuelaM,YildizBO,etal.COVID-19andendocrineandmetabolicdiseases.AnupdatedstatementfromtheEuropeanSocietyofEndocrinology.Endocrine.2021May;72(2):301-316.[28]RatnayakeGM,DworakowskaD,GrossmanAB.CanCOVID-19immunisationcausesubacutethyroiditis?[publishedonlineaheadofprint,2021Jul17].ClinEndocrinol2021.[29]RotondiM,CoperchiniF,RicciG,etal.JEndocrinolInvest.2021May;44(5):1085-1090.[30]RubinsteinTJ.ThyroidEyeDiseaseFollowingCOVID-19VaccineinaPatientWithaHistoryGraves'Disease:ACaseReport.OphthalmicPlastReconstrSurg.2021Nov-Dec01;37(6):e221-e223.[31]Saygılı ES,KarakilicE.SubacutethyroiditisafterinactiveSARS-CoV-2vaccine.BMJCaseRep.2021Oct1;14(10):e244711.[32]ShoenfeldY,Agmon-LevinN.'ASIA'-autoimmune/inflammatorysyndromeinducedbyadjuvants.JAutoimmun.2011Feb;36(1):4-8.[33]SigstadE,GrøholtKK,WesterheimO.SubacutethyroiditisaftervaccinationagainstSARS-CoV-2.TidsskrNorLaegeforen.2021Oct11;141(2021-14).[34]SiolosA,GartzonikaK,TigasS.ThyroiditisfollowingvaccinationagainstCOVID-19:Reportoftwocasesandreviewoftheliterature.MetabolOpen.2021Dec;12:100136.[35]SriphrapradangC.Aggravationofhyperthyroidismafterheterologousprime-boostimmunizationwithinactivatedandadenovirus-vectoredSARS-CoV-2vaccineinapatientwithGraves'disease.Endocrine.2021Nov;74(2):226-227.[36]SriphrapradangC,ShantavasinkulPC.Graves'diseasefollowingSARS-CoV-2vaccination.Endocrine.2021Dec;74(3):473-474.[37]Vera-LastraO,NavarroAO,DomiguezMPC,etal.TwoCasesofGraves'DiseaseFollowingSARS-CoV-2Vaccination:AnAutoimmune/InflammatorySyndromeInducedbyAdjuvants.Thyroid.2021Sep;31(9):1436-1439.[38]ZettinigG,KrebsM.TwofurthercasesofGraves'diseasefollowingSARS-Cov-2vaccination.JEndocrinolInvest.2021Aug3;1-2.[39]ZhangL,ZhuF,XieL,etal.ClinicalcharacteristicsofCOVID-19-infectedcancerpatients:AretrospectivecasestudyinthreehospitalswithinWuhan,China.Ann.Oncol.2020,31,894–901.作品原创,转载请注明作者信息及来源
 颜兵 主任医师 北京霍普医院 甲状腺核医学科2498人已读
颜兵 主任医师 北京霍普医院 甲状腺核医学科2498人已读 - 精选 复查甲状腺功能,早上吃优甲乐,还是不吃优甲乐,我们到底应该听谁的?
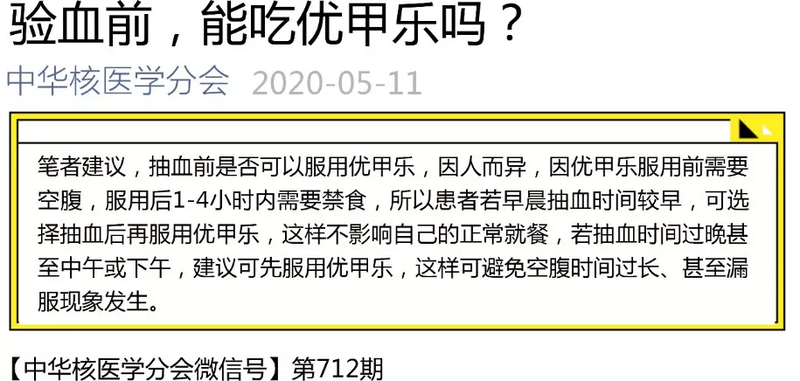
前言 我的患者经常问我一个问题:你告诉复查当天可以吃早餐,但是不能吃优甲乐(学名:左甲状腺素,英文名:Levothyroxine,英文缩写L-T4),但是其他专家,以及科普短文说可以吃优甲乐。你们都是大咖,我们到底应该听谁的? 对于偏执的、细节控的我,一定要搞清楚,给自己、给患者一个答案。但是很遗憾,这将是我的第一篇偏重于学术且没有答案的科“普”。虽然医学问题很复杂,可能现在还没有答案,但是,随着人类永不停止的探索,相信将来一定有一个答案。 昨天把这篇文章发给行业内大咖点评——写得很好,但这不像是科普,很烧脑! 的确,科而不普。但是,如果这篇科“普”所涉及的话题对您很重要,不妨看一看,或许能帮助你从中找到你自己的答案。 温馨提示:阅读全文将占据您宝贵的15分钟时间。 补充说明:甲状腺激素药物包括优甲乐(L-T4)、雷替斯(L-T4)、加衡(L-T4)、以及甲状腺素片(含T4和T3),文中提及的优甲乐泛指所有的左甲状腺素药物(L-T4)。 首先,检索相关科普短文,得到三篇具有影响力的科普短文: 科普短文-01 科普短文-02 科普短文-03 第一篇科普给出2个建议:①若早晨抽血时间较早(没有给予“较早”定义),可先抽血后吃优甲乐;②若抽血时间过晚(中午或下午),可先吃优甲乐后抽血。第二篇和第三篇科普观点一致,复查当天可以吃优甲乐,不影响医生对结果的判断。 难道我给患者的建议是不科学的吗? 缺乏证据的个人经验,甚至难以让自己完全信服,立即行动搜寻证据: ■ 重温优甲乐说明书(建议患者认真阅读说明书),看看能给我们什么样的提示 很显然,吃药后L-T4会逐渐被吸收,5-6小时后将上升至最高峰。理论上讲,这必然会导致血液中甲状腺激素水平升高,但说明书并没有给出短时间内甲状腺激素水平上升的幅度,以及达到高峰后下降情况,更没有给出L-T4暂时升高是否影响医生准确判断甲减患者吃药量? ■ 再看看科研文献怎么说 在Pubmed 文献数据库中检索,检索词:hypothyroidism(甲减)、thyroid hormone(甲状腺激素)、levothyroxine(左甲状腺素,L-T4)、free triiodothyronine(游离三碘甲状腺原氨酸,FT3)、 total triiodothyronine(总三碘甲状腺原氨酸,TT3)、free thyroxine(游离甲状腺素,FT4)、total thyroxine(总甲状腺素,TT4)、thyroid stimulating hormone(促甲状腺激素,TSH)。在上千篇文献中遴选出几十篇关于因甲状腺癌手术后、甲亢手术后、甲亢碘-131治疗后、以及其他原因的甲减患者早上吃优甲乐(L-T4)后连续测定血液中T3、T4、TSH的科研文献。 优甲乐(L-T4)的吸收情况 口服L-T4在胃内溶解后,主要在小肠吸收[1]。在甲状腺功能正常的志愿试验者中,L-T4吸收高峰出现在2小时,而甲减患者延后至3小时出现[2]。在甲状腺功能正常的志愿试验者中,大约60%-80%被吸收进入血液,甲减患者的吸收率略高于正常人[3]。有很多的因素可以影响甲状腺激素的吸收,如食物、其他药物、服用时间、胃肠道疾病等[1]。 早上吃优甲乐(L-T4)后抽血复查,对T3、T4、TSH测定结果有什么影响? 我在Pubmed文献库检索到的相关文献中,Saberi & Utiger的研究显示:成人甲减患者经甲状腺激素替代补充后,无论TSH已恢复正常的,还是TSH仍然高于正常的,口服100-200ug L-T4后,连续每2小时测定一次TT3、TT4、TSH结果没有变化[4]。另外,Czernichow等人报道先天性甲减的婴儿也没有观察到TT4的变化[5]。 除外上述寥寥的2篇文献,其他的研究结论与之截然相反。这种差异,Wennlund认为是由于Saberi & Utiger在1974年采用一种特异较差的竞争性蛋白结合试验测定TT4所致[4,6]。 其他文献的研究显示,口服L-T4后,血液中FT4或TT4在半小时后开始迅速升高[7,8]。2-4小时达到峰值(最高值)[5-19],升高幅度可达到10%-55%[6,8,10,12,19],且FT4升高幅度高于TT4升高[8,19]。美国甲状腺协会2014版《甲减治疗指南》中引用了Ain等人[19]的研究——在服用L-T4后4小时左右,血清T4和FT4水平将出现一个约15%的短暂峰值[20]。在接受L-T4抑制治疗的甲状腺癌患者中,TT4最大升幅16±2%,FT4最大升幅更高达22±3%[19]。 Symons、Deam、Ghosh等人[12,21,22]的研究还显示:①基础FT4较高的甲减患者,FT4上升幅度也较高;②口服L-T4剂量越大的甲减患者,FT4上升幅度也越高;③甲状腺激素水平低于正常的甲减患者,FT4升高幅度高于甲状腺激素替代补充后甲状腺激素水平处于正常的甲减患者。 当FT4和TT4达到峰值后逐渐下降,大约10-12小时后恢复至早上空腹未吃药时的基线水平[15,19]。在24小时内,T3水平不变或略升高,TSH水平保持不变或稍有降低[5,6,8,10,12,21]。 早上吃优甲乐(L-T4)后抽血复查,是否影响医生的判断? 由于口服L-T4后,不同时间抽血的TT4和FT4存在显著差异。Wennlund[6]认为:如果通过血液中甲状腺激素水平来调整甲状腺激素替代补充剂量,那么抽血时间就应该标准化。Wennlund[6]和Liewendahl[22]等人建议在任何情况下,检查结果的解释必须与抽血时间相结合。但是,由于受到不同时间升高幅度个体间显著差异的影响,Symons等人认为:对所有接受甲状腺素治疗的患者进行标准化采血是不切实际的[12]。Soppi[8]和Liewendahl[22]等人指出:口服甲状腺激素后L-T4对血液中TT4和FT4存在显著影响,检查结果的解释可能导致对甲状腺素替代补充剂量的错误判断。因此,建议先抽血,后吃药。 复查甲状腺功能,早上是吃优甲乐,还是不吃优甲乐? 甲状腺激素属于治疗范围狭窄类药物,药量轻微的波动可能导致敏感患者不适反应[23]。为此,2009年10月美国药典将药物效期内由每片含L-T4不少于标示量的90.0%,且不超过标示量的110.0%的标准提高至更严格的95%~105%[24]。由于甲减患者需要在狭窄的治疗范围内进行终生的甲状腺激素替代补充[25]。因此,对于患者每次抽血复查结果的正确解读十分重要,尤其对于需要TSH抑制性治疗的甲状腺癌患者更为重要。 美国甲状腺协会2015版《甲状腺结节和分化型甲状腺癌诊疗指南》推荐:高风险甲状腺癌患者的TSH抑制应维持在< 0.1mU/L,中风险患者的TSH抑制应维持在0.1–0.5 mU/L,低风险患者的TSH抑制应维持在0.5–2.5 mU/L[26]。 对于中、高风险甲状腺癌患者,TSH抑制在正常值以下,此时依靠TSH调整药物剂量已经变得不可能。此情况下,FT4水平比FT3水平更能准确地反映TSH反应,TSH对促甲状腺激素释放激素的反应程度与FT4的相关性好于与TT3和FT3的相关性[27],对于接受抑制性L-T4治疗的患者,更依赖于FT4水平来衡量甲亢的程度[19] 。 Ain等人认为:亚临床甲亢和临床甲亢之间可能存在一个狭窄的阈值,这可以通过准确测定FT4来寻找,FT4水平应尽可能保持在较低的水平,同时维持TSH抑制目标。口服L-T4后9小时内血液中甲状腺激素水平会短暂升高,准确评估应考虑到这种影响因素,这对于选择最小剂量的左旋甲状腺素抑制促甲状腺素具有重要意义[19]。Maxon等人认为:口服L-T4之前抽血检查,可以更准确地评估给定剂量下获得的平均FT4水平,特别是对于接受抑制剂量L-T4治疗的甲状腺癌患者[15]。 【结束语】 如果早上吃优甲乐(L-T4)后复查,由于血液中FT4和TT4迅速升高,2-4小时后达到高峰值,10-12小时后又缓慢下降回到基线水平,这对于通过复查甲状腺功能来准确判断甲减患者甲状腺激素补充剂量带来了困惑,尤其是对TSH抑制治疗的甲状腺癌患者。加之患者之间的个体差异性,使得这种变化变得更加复杂,即便是有经验的甲状腺专科医生,也可能导致患者反复调药,频繁复查。 参考文献 [1] Skelin M, Lucijanic T, Amidzic Klaric D, Resic A, Bakula M, Liberati-Cizmek AM, Gharib H, Rahelic D. Factors Affecting Gastrointestinal Absorption of Levothyroxine: A Review. Clin Ther, 2017, 39:378-403. [2] S Benvenga, L Bartolone, S Squadrito, F Lo Giudice, F Trimarchi. Delayed intestinal absorption of levothyroxine. Thyroid. 1995 Aug; 5(4): 249-53. [3] Philippe Colucci, Corinne Seng Yue, Murray Ducharme, Salvatore Benvenga. A Review of the Pharmacokinetics of Levothyroxine for the Treatment of Hypothyroidism. Eur Endocrinol. 2013 Mar; 9(1): 40-47. [4] Saberi M, Utiger RD. Serum thyroid hormone and thyrotropin concentrations during thyroxine and triiodothyronine therapy. J Clin Endocrinol Metab. 1974 Nov; 39(5):923-7. [5] P Czernichow, B Wolf, J Fermanian, R Pomarede, R Rappaport. Twenty-four hour variations of thyroid hormones and thyrotrophin concentrations in hypothyroid infants treated with L-thyroxine. Clin Endocrinol (Oxf). 1984 Oct; 21(4): 393-7. [6] A Wennlund. Variation in serum levels of T3, T4, FT4 and TSH during thyroxine replacement therapy. Acta Endocrinol (Copenh), 1986 Sep; 113(1): 47-9. [7] A Carpi, M G Toni, C De Gaudio. Effect of a single oral dose of L-thyroxine (150 micrograms) on serum thyroid hormone and TSH concentrations in clinically euthyroid goitrous patients. Thyroidology. 1992 Aug; 4(2): 69-73. [8] E Soppi, K Irjala, H L Kaihola, J Viikari. Acute effect of exogenous thyroxine dose on serum thyroxine and thyrotrophin levels in treated hypothyroid patients. Scand J Clin Lab Invest. 1984 Jun; 44(4): 353-6. [9] D G Read, M T Hays, J M Hershman. Absorption of oral thyroxine in hypothyroid and normal man. J Clin Endocrinol Metab. 1970 Jun; 30(6):798-9. [10] M I Surks, A R Schadlow, J H Oppenheimer. A new radioimmunoassay for plasma L-triiodothyronine: measurements in thyroid disease and in patients maintained on hormonal replacement. J Clin Invest. 1972 Dec; 51(12):3104-13. [11] Wenzel KW, Meinhold H. Evidence of lower toxicity during thyroxine suppression after a single 3-mg L-thyroxine dose: comparison to the classical L-triiodothyronine test for thyroid suppressibility. J Clin Endocrinol Metabol. 1974; 38: 902-905. [12] Symons RG, Murphy LJ. Acute changes in thyroid function tests following ingestion of thyroxine. Clin Endocrinol (Oxf). 1983 Oct; 19(4): 539-46. [13] Valente WA, Goldiner WH, Hamilton BP, Wiswell JG, Mersey JH. Thyroid hormone levels after acute L-thyroxine loading in hypothyroidism. J Clin Endocrinol Metab. 1981; 53: 527-529. [14] Stone E, Leiter LA, Lambert JR, Silverberg JDH, Jeejeebhoy KN, Burrow GN. L-Thyroxine absorption in patients with short bowel. J Clin Endocrinol Metab. 1984; 59: 139-141. [15] Maxon H, Voile C, Hertzberg V, Chen I-W, Fernandez-Ulloa M. Clin Nucl Med. Variations in serum thyroxine concentrations with time after an oral replacement dose. 1987 May; 12(5): 389-90. [16] M.T. Hays, Thyroid hormone and the gut. Endocr. Res. 14(2-3), 203–224 (1988) [17] Sturgess I, Thomas SH, Pennell DJ, Mitchell D, Croft DN. Diurnal variation in TSH and free thyroid hormones in patients on thyroxine replacement. Acta Endocrinol (Copenh). 1989 Nov; 121(5): 674-6. [18] M.T. Hays, Localization of human thyroxine absorption. Thyroid 1(3), 241–248 (1991) [19] Ain KB, Pucino F, Shiver TM, Banks SM. Thyroid hormone levels affected by time of blood sampling in thyroxine-treated patients. Thyroid. Summer 1993; 3(2):81-85. [20] Jacqueline Jonklaas, Antonio C Bianco, Andrew J Bauer, Kenneth D Burman, Anne R Cappola, Francesco S Celi, David S Cooper, Brian W Kim, Robin P Peeters, M Sara Rosenthal,Anna M Sawka,American Thyroid Association Task Force on Thyroid Hormone Replacement. Guidelines for the treatment of hypothyroidism: prepared by the American thyroid association task force on thyroid hormone replacement.Thyroid.2014 Dec; 24(12):1670-751. [21] D R Deam,D G Campbell,S Ratnaike. Effect of oral intake of thyroxine on results of thyroid function tests in patients receiving thyroid replacement therapy.Med J Aust.1983 Oct 15; 2(8): 374-6. [22] Sujoy Ghosh,Subhodip Pramanik,Kaushik Biswas,Kingshuk Bhattacharjee,Rajib Sarkar,Subhankar Chowdhury,Pradip Mukhopadhyay.Levothyroxine Absorption Test to Differentiate Pseudomalabsorption from True Malabsorption.Eur Thyroid J.2020 Jan; 9(1): 19-24. [23] Blakesley VA. Current methodology to assess bioequivalence of levothyroxine sodium products is inadequate. AAPS J, 2005, 7: E42–6. [24]The United States Pharmacopeial Convention. Current USP monograph of Levothyroxine Sodium Tablets (published in Revision Bulletin, Official February 1, 2010).2009. [25] Ilgin Yildirim Simsir,Utku Erdem Soyaltin,Ahmet Gokhan Ozgen. Levothyroxine absorption test results in patients with TSH elevation resistant to treatment.Endocrine.2019 Apr; 64(1): 118-121. [26] 2015 American Thyroid Association Management Guidelines for Adult Patients with Thyroid Nodules and Differentiated Thyroid Cancer: The American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. Thyroid. 26(1), 1–133 (2016). [27]S Ryder,G M Gollapudi,A Varma. Relationship of serum T4 and T3 to TSH in primary hypothyroidism.Arch Intern Med.1980 Oct; 140(10):1290-1. 注:本文为北京霍普医院 颜兵医生原创文章,如有转载请注明出处。
 颜兵 主任医师 北京霍普医院 甲状腺核医学科1271人已读
颜兵 主任医师 北京霍普医院 甲状腺核医学科1271人已读 - 精选 甲状腺癌碘-131治疗后是否显著增加了第二癌症风险?
源自"甲状腺癌碘-131治疗后是否显著增加了第二癌症风险?"视频文字整理1. 其实关于“甲状腺癌碘-131治疗后是否显著增加了第二癌症风险”这期视频,我录制了两次,第一次录制之后,我自己也不是太有把握患者是否能够听明白,因此我没有直接上传视频,而是先发给几位甲癌患者先看一看,希望能得到他们的反馈意见。2. 有患者反映没有完全搞清楚,尤其是其中的一些专业术语。为此,我根据他们的建议,又重新录制了一次,希望这一次能把这个问题讲清楚。3. 视频的时间相对较长,如果感兴趣的患者,得有一点耐心把视频看完,希望能解答各位的疑惑。4. 我将从以下两个视角给大家深入讲解。第一个视角:先从已发表的文献来看一下,全世界各位学者的研究结果是怎么的?· 有一些的文献认为碘-131治疗后第二癌症风险显著增高,但也有文献报道没有发现风险增高,甚至有的文献报道某些恶性肿瘤风险反而降低了。· 虽然我一直从事甲状腺疾病的诊疗工作,但是我自己看了这些结论不一致的文献也感觉有些迷惑,我估计患者更加蒙圈。· 我这段时间恰巧与北京协和医院林岩松教授一起写一本《甲状腺癌全程管理》的新书,其中我写关于辐射防护相关内容,我正好可以深入研究了一下产生这些研究结论不一致原因。从我所浏览的文献来看,主要受到以下一些混杂因素的影响:1)患有恶性肿瘤的患者,一生中发生第二癌症的风险显著高于普通人群· 1973~2000年美国癌症登记数据显示,与普通人群比较,恶性肿瘤患者中发生第二甲状腺癌的相对风险度(risk ratio,RR)显著增加,RR=1.42倍;甲状腺癌患者中发生非甲状腺的第二癌症的相对风险度也同样显著增加了,RR=1.39倍[1]。· 有学者认为所有癌症患者,发生第二癌症的相对风险度显著升高,RR=2倍[2]。· 有研究报道,如果患者存在多器官癌症易感基因,例如患者有CHEK2癌症易感基因,那么患者患上甲状腺癌的相对风险度(RR)=4.9倍、乳腺癌RR=2.2倍、前列腺癌RR=2.2、肾癌RR=2.1、结肠癌RR=2.0[3]。· 如果将甲状腺癌碘-131治疗患者与普通人群进行比较,必然会得到风险显著增高的结论。由于没有剔除甲状腺癌患者本身第二癌症的高发生率所致癌症,从而导致高估了碘-131治疗后第二癌症风险,显然这种科研设计不科学。· 如果将甲状腺癌碘-131治疗患者与甲状腺癌手术后没有碘-131治疗患者进行比较,则风险没有显著增高。2)第二癌症的定义和随访观察时间· 有的文献定义碘-131治疗后6个月后发生的癌症为第二癌症,有的定义为碘-131治疗后1年后,也有2年的,最长的为3年后。· 目前研究认为某种危险因素导致白血病的发生需要5-6时间后,除外血液系统发生的其他癌症,也称实体癌症的发生需要10年时间后[4]。· 这些癌症如果在碘-131治疗后2-3年内被发现,这就很难区分是与碘-131有关,或者是甲状腺癌患者隐匿的癌症因频繁的体检提前发现了。如果把这些归因于碘-131治疗相关,这也势必会高估碘-131治疗后第二癌症发生风险。· 但如果随访时间太短,仅几年时间,这时还没有观察到癌症的发生,这时可能会得到风险没有增加,从而也存在可能低估碘-131治疗后第二癌症风险。相反,如果偶然出现一个第二癌症,则可能提示风险显著增高,这样以来随访观察时间太短,同样也会显著影响研究结果。3)纳入研究患者的数量由于各种癌症的发生率都相对较低,研究结果很容易受到研究患者数量的影响。举一个极端的例子,如果研究的患者数量只有1人,如果发生1例第二癌症,则发生率为100%;如果是100个人,则发生率是1%,如果是1000人,则发生率为0.1%。由于目前的研究文献多数为小样本研究,其结论受到样本数量局限性影响,从而使得结论的可信度降低。4)纳入研究患者的病情并非所有甲状腺癌手术后都需要碘-131治疗。但是,手术后需要碘-131治疗患者的病情往往较不做碘-131治疗患者的病情更严重,如肿瘤恶性度更高、淋巴结转移更多、发生甲状腺腺外侵犯、以及发生肺转移、骨转移等远处转移。显然,他们发生第二癌症的风险性可能高于不作碘-131治疗的甲状腺癌患者,这也势必高估碘-131治疗后第二癌症风险,显然这样的结论可信度不高。结论:· 目前还没有令人信服的证据表明甲状腺癌碘-131治疗后第二癌症风险显著增高。· 如果将来最终数据证明碘-131治疗可以导致第二癌症风险增高,那么我估计也可能是略微增高。· 但如果真的是显著升高,那么现有的研究早已经得到一致性研究结果。第二个视角:我从另外一个视角来看碘-131治疗是否导致第二癌症的风险增高。· 碘-131治疗时,除外唾液腺、胃、肾脏和膀胱,患者全身所受到的辐射剂量大约200 mSv(毫希沃特)左右,相当于患者做了20次CT检查所受到的辐射剂量。· 200mSv的辐射剂量看上去较高,其实低于1000mSv仍然是低剂量辐射[5]· 假设接受一次这个样的低剂量辐射就可能显著增加致癌风险。如果是这样,那么生活在全世界天然本底辐射最高的地区——伊朗拉姆萨尔(Ramsar),当地居民每年受到的辐射剂量是260mSv [6],相当于从受精卵开始,每个月做了2次CT,或者相当于每年做了一次碘-131治疗。· 在此,我们可以试想一下,比全世界平均天然辐射水平高100倍的Ramsar,一定是一个世界上癌症发生率最高发地区,很多人将死于癌症。· 但实际的情况恰恰相反,Ramsar地区的居民癌症发生率以及寿命与伊朗其它地区没有差别[7, 8]。· 这么高的辐射,为什么癌症风险没有增加?· 人类生活的星球,从远古时代开始,就有存在大量放射性物质,人类早已建立了一套防御辐射的体系,可以修复因辐射损伤的DNA,和清除不能修复的DNA,因此不会因为低剂量辐射而导致癌症风险增高[9-11]。· 有文献报道,低剂量辐射不但不会致癌,反而会有益于健康,激发机体免疫力,使得癌症发生率降低。这种现象在许多国家得到印证,例如中国广东阳江地区的天然本底辐射是6.4msv,是中国其它地区的3倍剂量,但是该地区人的癌症发生率更低,寿命反而更长[12, 13]。结论:正是因为人类具有强大的自我辐射损伤修复能力,使人类在有辐射环境中能够继续繁衍[14, 15]。碘-131应用于甲状腺癌治疗已近80年历史,仍然没有确凿数据能证明第二癌症风险增高,或许正是人类辐射损伤的修复机制发挥了作用。参考文献[1] Ronckers CM, McCarron P, Ron E.Thyroid Cancer and Multiple Primary Tumors in the SEER Cancer Registries. Int J Cancer, 2005, 117(2): 281-288.[2] Rheingold SR, Neugut AI, Meadows AT. Secondary cancers: incidence, risk factors, and management. In: Bast RC , Jr, Kufe DW, Pollock RE, et al., eds, Holland-Frei Cancer Medicine, 5th edn, Chapter 156. Hamilton, ON: BC Decker INC, 2000.[3] Cybulski C, Gorski B, Huzarski T, et al. CHEK2 is a multiorgan cancer susceptibility gene. Am J Hum Genet, 2004, 75(6):1131-1135.[4] Dahal S, Budoff M J. Low-dose Ionizing Radiation and Cancer Risk: Not So Easy to Tell. Quant Imaging Med Surg, 2019, 9(12): 2023-2026.[5] Sutou S. Black Rain in Hiroshima: A Critique to the Life Span Study of A-bomb Survivors, Basis of the Linear No-Threshold Model. Genes Environ, 2020, 42, 1.[6] Mortazavi S, Ghiassi-Nejad M, Karam P, et al. Cancer incidence in areas with elevated levels of natural radiation. International Journal of Low Radiation, 2005, 2: 20-27.[7] Mortazavi S, Mozdarani H. Is it time to shed some light on the black box of health policies regarding the inhabitants of the high background radiation areas of Ramsar. Int J Radiat Res. 2012, 10: 111-116.[8] Mortazavi S, Mozdarani H. Non-linear phenomena in biological findings of the residents of high background radiation areas of Ramsar. Int J Radiat Res, 2013, 11: 3-9.[9] Luckey TD. Radiation Hormesis. Boca Raton, FL: CRC Press, 1991.[10]Aurengo A, Averbeck D, Bonnin A, et al. Dose Effect Relationships and Estimation of the Carcinogenic Effects of Low Doses of Ionizing Radiation. Paris, France: Acad′ emie des Sciences-Acad′ emie nationale de M′ edecine, March 2005.[11] Sacks B, Meyerson G, Siegel J A. Epidemiology without biology: false paradigms, unfounded assumptions, and specious statistics in radiation science (with commentaries by Inge Schmitz-Feuerhake and Christopher Busby and a reply by the authors). Biol Theory, 2016, 11: 69-101.[12] Z Tao Z, Y, S,et al. Cancer Mortality in the High Background Radiation Areas of Yangjiang, China During the Period Between 1979 and 1995. J Radiat Res, 2000, 41 Suppl, 31-41.[13] 潘自强, 郭明强, 崔广志, 等. 中国天然辐射本底水平和居民剂量估算. 辐射防护, 1992, 12(4): 251-259.[14] Jaworowski Z. Beneficial effects of radiation and regulatory policy. Australas Phys Eng Sci Med, 1997, 20(3): 125-138.[15] Karam P A, Leslie S A. Calculations of background beta-gamma radiation dose through geologic time. Health Phys, 1999, 77(6): 662-667.
颜兵 主任医师 北京霍普医院 甲状腺核医学科9697人已读
问诊记录 查看全部
- 甲状腺4c类结节 上次甲状腺水平和这次相差有点大,辛苦医生帮忙看一下用药量和这... 两次甲状腺水平相差较大,药量是否调整,有没有甲减或者甲亢,需要调整什么总交流次数2已给处置建议
- 甲状腺癌全切右清26/50,需要二次碘? 术后复查PET/ CT显示咽旁间隙有结节 ①2023年4月7日确诊甲状腺有问题,在之前没有明显的症状。... 想您帮我分析我这个情况能观察?还是说要抓紧时间去手术,找了几个超声医生都看不到咽部那个结节,无法穿刺...总交流次数18已给处置建议
- 甲状腺结节 有痰咳不出,感觉有东西往嗓子流动,本来想查个喉镜,随口说脾气... 请问医生这种情况是否严重?要手术吗?还是定期复查?总交流次数12已给处置建议
- 查出甲状腺问题三年了。喉咙有梗咀感。 甲状腺结节21年单位体检时查到的,当时报的是三类。喉咙一直异... 请主任帮我看下这个报告有什么问题?有什么专业建议可以给到我。总交流次数13已给处置建议
- 甲状腺癌手术后复查 甲状腺癌已经治愈后各项指标正常,想怀孕。 您好,甲状腺癌已经治愈,可以做试管婴儿怀孕吗?总交流次数3已给处置建议



